「触る」ことが痛みに?
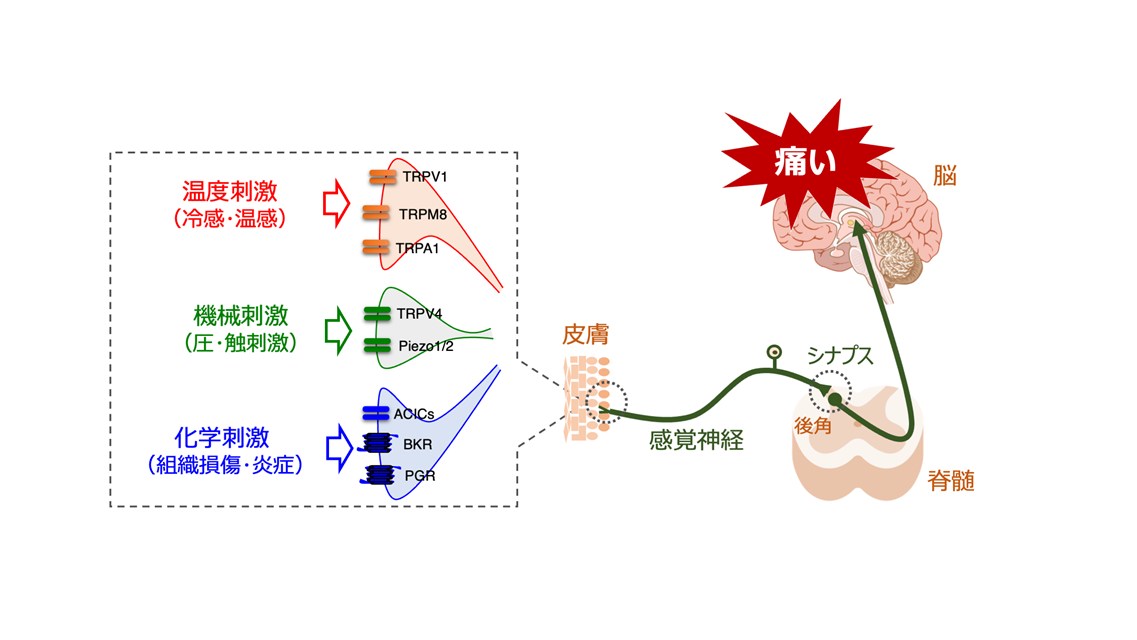
痛みは本来、けがや異常を知らせる大切なサインです。皮膚の受容器が温度・機械・化学刺激を感知し、その情報が神経を介して脊髄から脳へと伝達され、「痛み」として認識されます(図1)。
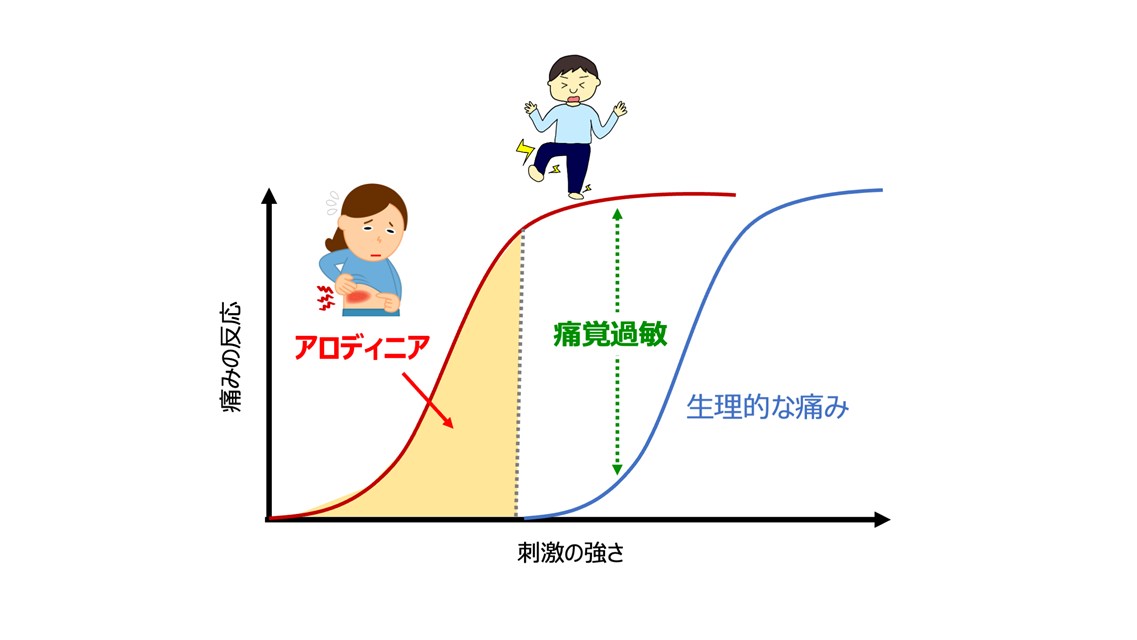
しかし、神経が損傷すると、衣服が触れるだけで強い痛みを感じることがあります。これは神経障害性疼痛と呼ばれ、糖尿病やがん、帯状疱疹、脊髄損傷などに伴って発症します(図2)。本来は痛みを伴わないはずの触覚が、痛みとして伝わるのです。
神経障害性疼痛は慢性化しやすく、既存の鎮痛薬が十分効かないことや副作用の問題もあるため、新たな作用機序に基づく治療法の開発が求められています。
しかし、神経が損傷すると、衣服が触れるだけで強い痛みを感じることがあります。これは神経障害性疼痛と呼ばれ、糖尿病やがん、帯状疱疹、脊髄損傷などに伴って発症します(図2)。本来は痛みを伴わないはずの触覚が、痛みとして伝わるのです。
神経障害性疼痛は慢性化しやすく、既存の鎮痛薬が十分効かないことや副作用の問題もあるため、新たな作用機序に基づく治療法の開発が求められています。
痛みの「スイッチ」と「ブレーキ」を探る
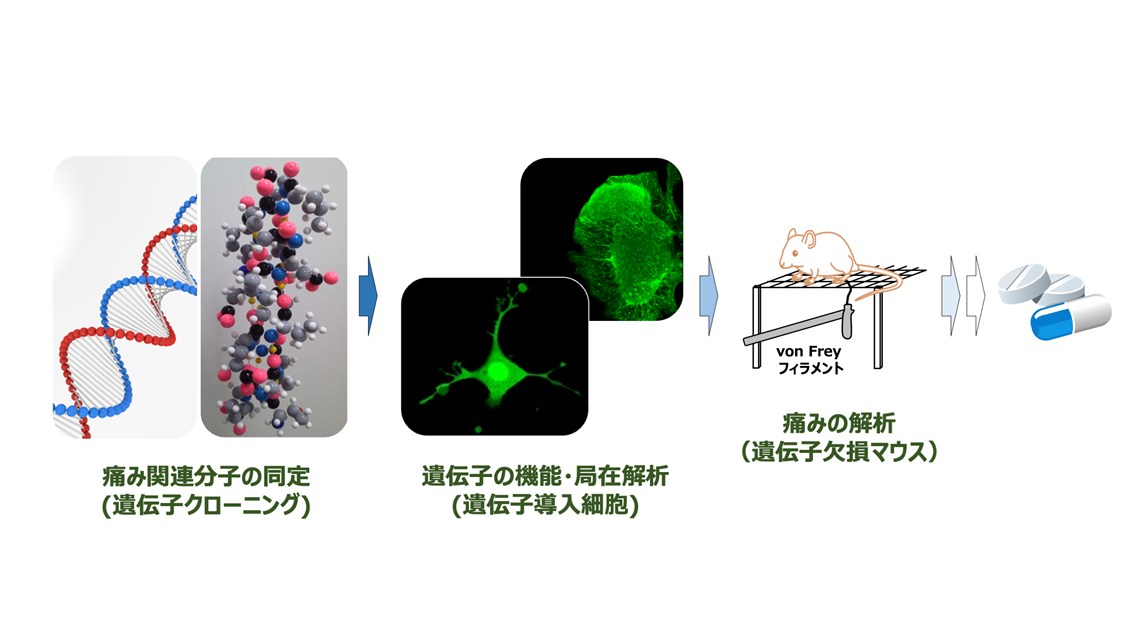
痛みの情報伝達を制御する神経ペプチドに注目し、「触刺激がなぜ痛みに変わるのか」を研究しています。神経ペプチドは神経細胞が分泌する生理活性物質で、神経機能を調節します。遺伝子改変マウスの行動解析や分子生物学的手法、さらには工学的技術も組み合わせ、分子・細胞・神経回路・個体行動という多階層から痛みのメカニズムを解析しています(図3)。
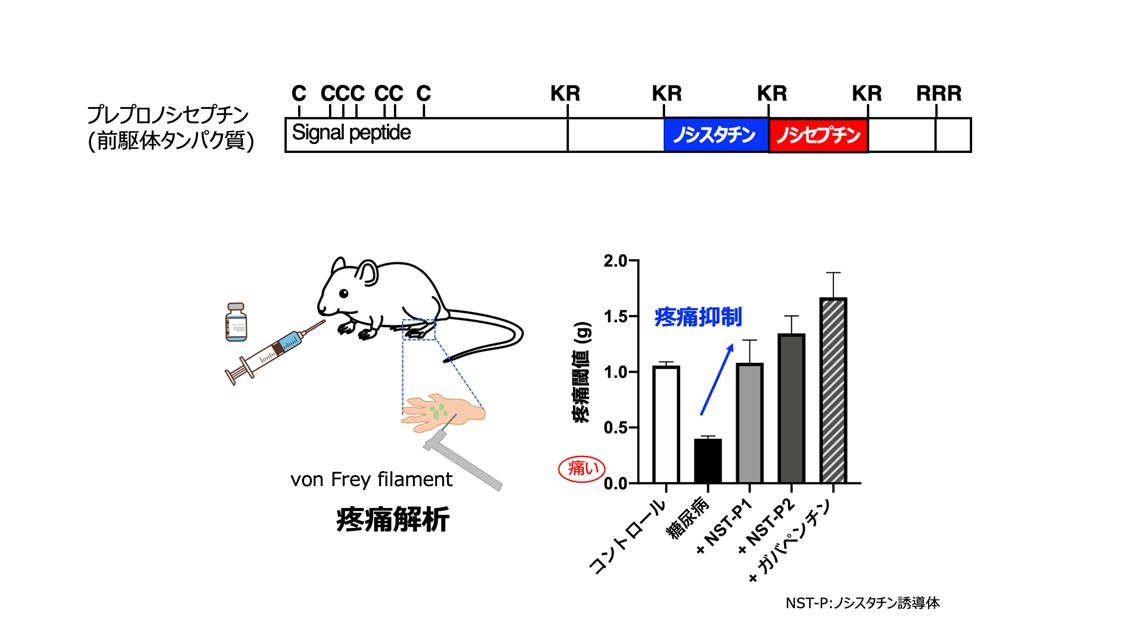
その結果、神経ペプチドであるノシセプチン/オーファニンFQ(N/OFQ)をマウスの髄腔内に投与すると、触刺激で痛みを生じるアロディニアが誘発されることを見出しました。一方、同じ前駆体から産生されるノシスタチン(NST)には、このアロディニアを抑制する作用があり、「痛みのブレーキ」として働きます。
現在は、ノシスタチンの構造を改変した誘導体を設計・合成し、経口投与が可能で、副作用の少ない新しい鎮痛薬の開発を進めています(図4)。
その結果、神経ペプチドであるノシセプチン/オーファニンFQ(N/OFQ)をマウスの髄腔内に投与すると、触刺激で痛みを生じるアロディニアが誘発されることを見出しました。一方、同じ前駆体から産生されるノシスタチン(NST)には、このアロディニアを抑制する作用があり、「痛みのブレーキ」として働きます。
現在は、ノシスタチンの構造を改変した誘導体を設計・合成し、経口投与が可能で、副作用の少ない新しい鎮痛薬の開発を進めています(図4)。
難病に伴う慢性疼痛の解明へ
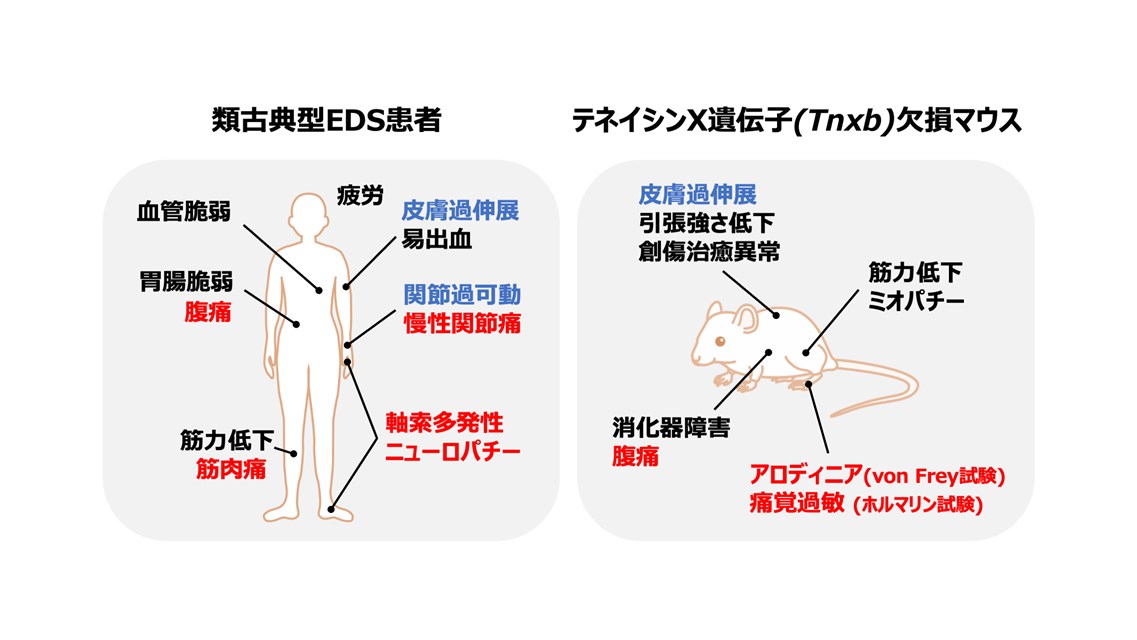
エーラス・ダンロス症候群(EDS)は、約5,000人に1人にみられる遺伝性結合組織疾患で、指定難病に認定されています。皮膚がよく伸びる、関節が柔らかすぎるなどの症状に加え、患者の約90%が慢性的な痛みに悩まされています(図5)。
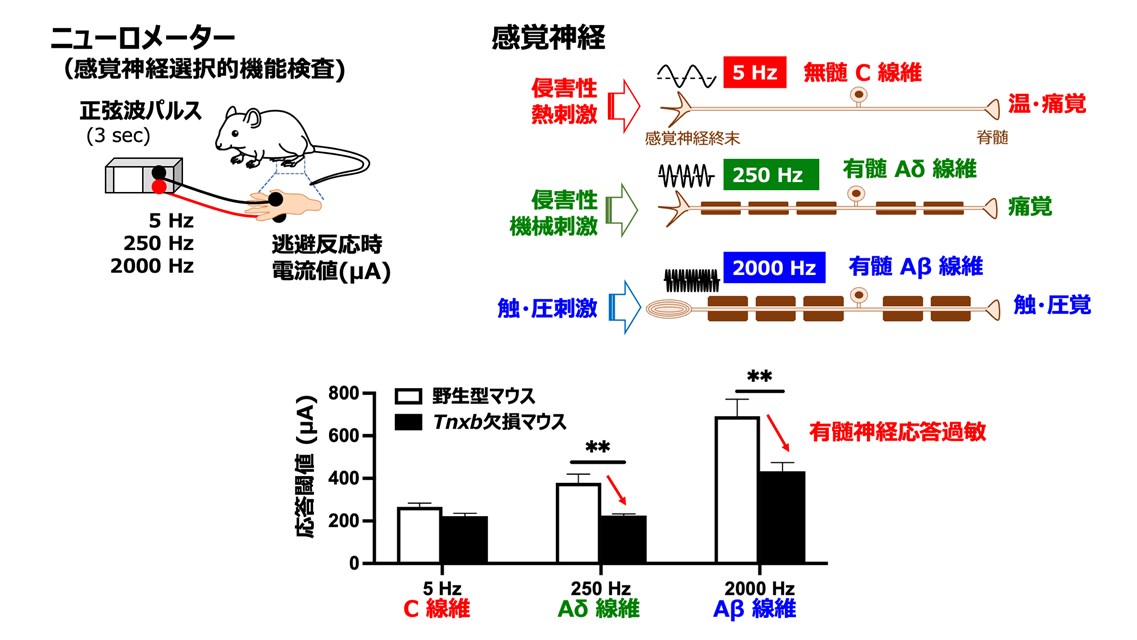
EDSの原因遺伝子の一であるテネイシンX(Tnxb)を欠損したマウスを用いた解析から、有髄神経の過敏化が神経障害性疼痛を引き起こすことを明らかにしました(図6)。これは、「体を支える結合組織の異常が神経機能に影響し、慢性疼痛を誘導する」という新しい病態メカニズムを示す成果です。
EDSの原因遺伝子の一であるテネイシンX(Tnxb)を欠損したマウスを用いた解析から、有髄神経の過敏化が神経障害性疼痛を引き起こすことを明らかにしました(図6)。これは、「体を支える結合組織の異常が神経機能に影響し、慢性疼痛を誘導する」という新しい病態メカニズムを示す成果です。
基礎科学の視点から痛みの本質に迫り、その知見を次世代の治療法へとつなげることが、私たちの目標です。
詳しい研究内容は、研究室オリジナルサイトをご覧ください。
詳しい研究内容は、研究室オリジナルサイトをご覧ください。